Schlüssel zur Trickkiste der Bakterien
20.08.2020Einem Würzburger Forschungsteam ist erstmals die RNA-Einzelzellsequenzierung bei Bakterien gelungen. Die Studie ist im Fachmagazin Nature Microbiology veröffentlicht.
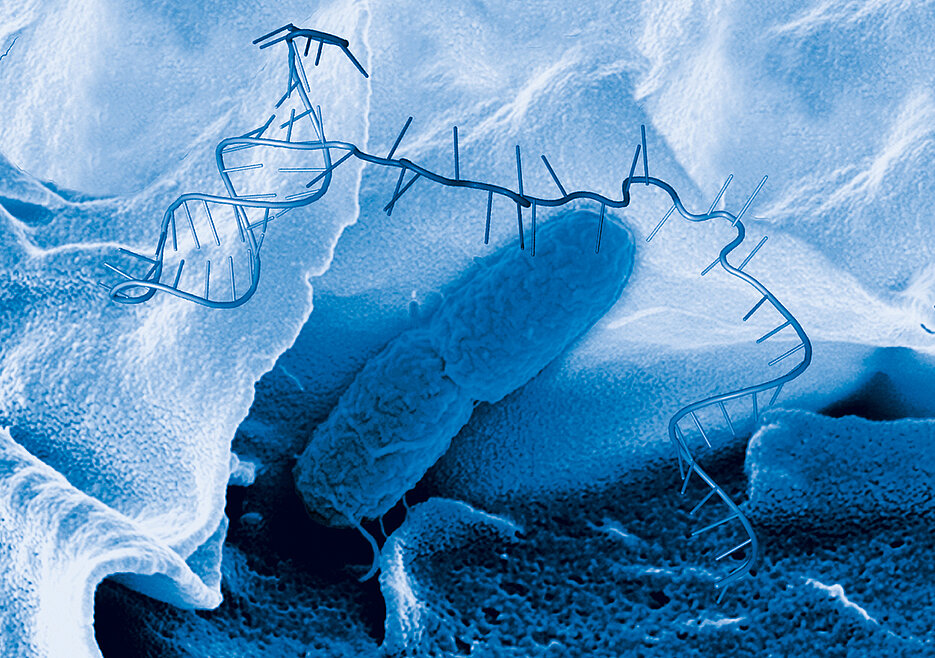
Unter Millionen Bakterien gibt es immer einzelne, die sich von einer Antibiotika-Behandlung oder unserem Immunsystem unbeeindruckt zeigen. Das ist eine der großen Herausforderungen in der Infektionsmedizin.
Wie sich die Aktivität von Genen in individuellen Bakterien mit einem neuen Verfahren bestimmen lässt, zeigt nun ein Forschungsteam des Würzburger Helmholtz-Instituts für RNA-basierte Infektionsforschung (HIRI), einem Standort des Helmholtz-Zentrums für Infektionsforschung (HZI), im Fachmagazin Nature Microbiology.
Mit dem neuen Verfahren der bakteriellen RNA-Einzelzellsequenzierung könnte man künftig herausfinden, welche Tricks Bakterien zur Ausbildung von Resistenzen nutzen, und diese Schlupflöcher mit passgenauen Medikamenten verschließen.
„Auch unter Bakterien gibt es Individualisten“, sagt Professor Jörg Vogel, Direktor des HIRI und gleichzeitig Vorstand des Instituts für molekulare Infektionsbiologie der Julius-Maximilians-Universität Würzburg (JMU). „Sie heben sich von der Masse ihrer genetisch identischen Artgenossen ab und trotzen lebensbedrohlichen Bedingungen, wie etwa dem Einfluss eines Antibiotikums.“ Wie genau sie das schaffen und welche Eigenschaften diese Individuen aus bakterieller Sicht zu Superhelden machen, ist bislang nicht verstanden.
Was man unter RNA-Einzelzellsequenzierung versteht
Das Forschungsteam um Jörg Vogel und Dr. Emmanuel Saliba, Leiter der HIRI-Arbeitsgruppe Einzelzellanalyse, ist mit seiner aktuellen Studie hier einen großen Schritt vorangekommen: Es ist ihm gelungen, einzelne Bakterien mithilfe der sogenannten RNA-Einzelzellsequenzierung zu untersuchen. Doch was muss man sich darunter vorstellen und welche Informationen liefert diese Methode?
In einem Bakterium sind nicht immer alle Gene aktiv, aber immer diejenigen, die für den Stoffwechsel unter den jeweils herrschenden Bedingungen notwendig sind. Der genetische Code eines aktivierten Gens wird in RNA (englisch: ribonucleic acid) umgeschrieben. Die RNA wiederum dient als Vorlage für die Herstellung von Proteinen, die bestimmte Funktionen innerhalb der Zelle erfüllen.
„Die Gesamtheit der in einem Bakterium vorhandenen RNA – das sogenannte Transkriptom – zeigt daher genau an, was zu diesem Zeitpunkt und den gegebenen Umständen notwendig ist, um zu überleben“, sagt Saliba. „Wenn es uns gelingt, das Transkriptom eines Bakteriums zu analysieren, das sich erfolgreich gegen eine antibiotische Behandlung durchsetzt, können wir tiefer in seine Trickkiste schauen.“
Warum die Methode bei Bakterien bisher nicht gelang
Die RNA-Einzelzellsequenzierung (englisch: single-cell RNA-seq) ist für Zellen eukaryotischer Organismen, zu denen der Mensch, Tiere und Pilze gehören, bereits etabliert. Bei Bakterien aber gelang sie bisher nicht.
Der Grund dafür: Die RNA eukaryotischer Zellen weist an einem Ende eine kurze Kette aus hintereinandergeschalteten RNA-Bausteinen namens Adenosin – kurz A genannt – auf. „Dieser Poly-A-Schwanz ist für das bisherige Verfahren der RNA-Einzelzellsequenzierung der entscheidende Ansatzpunkt für die Isolierung der RNA“, sagt Saliba. „Bei der bakteriellen RNA gibt es aber keinen Poly-A-Schwanz. Daher war eine Analyse der RNA einzelner Bakterien bisher nicht möglich."
Eine Bakterienzelle besitzt darüber hinaus auch nur sehr geringe Mengen an RNA, nämlich im Femtogramm-Bereich (billiardstel Gramm). Das erschwert die Detektion und Isolation bakterieller RNA zusätzlich. Das HIRI-Team hat in seiner Studie daher ein Poly-A-unabhängiges Verfahren namens MATQ-seq (englisch: multiple annealing and dC-tailing-based quantitative single-cell RNA-seq) genutzt. Hier wird die bakterielle RNA auf andere Weise gewonnen und kontrolliert vermehrt, sodass die RNA-Menge für eine anschließende Analyse und die Erstellung eines RNA-Profils ausreicht.
Salmonellen unter Stress gesetzt
In ihren Untersuchungen haben die HIRI-Forscher Bakterien der gut bekannten Gattung Salmonella unterschiedlichen Stressbedingungen ausgesetzt. Eine Probe wurde einem Salzschock ausgesetzt, eine andere unter Sauerstoffabschluss gesetzt. Anschließend haben die Wissenschaftler mithilfe der neuartigen Methode der RNA-Einzelzellsequenzierung die jeweiligen RNA-Profile erstellt und mit RNA-Profilen von Salmonella-Kulturen aus einer Datenbank verglichen, die zuvor denselben Stressbedingungen ausgesetzt waren.
„Salmonella diente in unserer Studie als Modellorganismus. Wir wollten prüfen, ob unsere Methode funktioniert“, sagt Vogel. „Und das tut sie – die RNA-Profile aus unseren Untersuchungen stimmten mit denen aus der Datenbank überein.“ Dass die RNA-Einzelzellsequenzierung nun auch für Bakterien funktioniert, eröffne ganz neue Möglichkeiten in der infektionsbiologischen Forschung.
„Wir sind mit der RNA-Einzelzellsequenzierung einen großen Schritt vorangekommen, um bakterielle Krankheitserreger und die Entstehung von Antibiotika-Resistenzen besser zu verstehen und mögliche Ansatzpunkte für wirksame Medikamente zu finden“, sagt Vogel. Das Verfahren funktioniere auch bei Pseudomonaden, also Bakterien, die die Lunge besiedeln.
Publikation
Fabian Imdahl*, Ehsan Vafadarnejad*, Christina Homberger, Antoine-Emmanuel Saliba#, Jörg Vogel#: Single-cell RNA-sequencing reports growth-condition-specific global transcriptomes of individual bacteria. Nature Microbiology 2020, doi: 10.1038/s41564-020-0774-1. (* trugen zu gleichen Teilen bei, # korrespondierende Autoren)