Kleiner Schalter mit großem Effekt
05.10.2020Winzige Veränderungen in Immunzellen können die Immunantwort spürbar verändern. Das haben Wissenschaftler der Universität Würzburg jetzt entdeckt. Ihre Erkenntnisse könnten für die Stammzelltherapie von Bedeutung sein.
Im menschlichen Immunsystem nehmen T-Zellen eine wichtige Rolle ein. Sie können krankes oder fremdes Gewebe mit großer Exaktheit von gesundem und eigenem Gewebe unterscheiden; sie können die notwendigen Maßnahmen vorantreiben, mit denen der Körper sich von den Störenfrieden befreit. Die Details dieser Immunantwort sind vielgestaltig; ihre einzelnen Schritte sind noch längst nicht bis ins Letzte verstanden.
Wissenschaftlerinnen und Wissenschaftler der Universitäten Würzburg und Mainz haben jetzt neue Einzelheiten dieser Vorgänge entschlüsselt. Demnach können winzige Punktmutationen in einem Gen die T-Zellen so verändern, dass sie einen Teil ihrer Aggressivität verlieren. Das könnte beispielsweise nach einer Stammzelltransplantation von Vorteil sein, bei der T-Zellen mitübertragen werden, um so eine Reihe gefürchteter Nebenwirkungen in Schach zu halten. Die Ergebnisse ihrer Arbeit haben die Forscher jetzt in der aktuellen Ausgabe der Fachzeitschrift Journal of Experimental Medicine veröffentlicht. Verantwortlich für die Studie ist Dr. Friederike Berberich-Siebelt, Leiterin der Forschungsgruppe „Molekulare und zelluläre Immunologie“ am Institut für Pathologie der Julius-Maximilians-Universität Würzburg (JMU).
Proteinfamilie mit vielen Aufgaben
Wenn T-Zellen fremdes oder verändertes Gewebe – wie beispielsweise eine Infektion oder Tumorgewebe – wahrnehmen, geschieht dies in der Regel über die Rezeptoren, die sie auf ihrer Zelloberfläche tragen. Diese T-Zell-Rezeptoren senden dann Signale in das Zellinnere und leiten auf diesem Weg eine Reaktion ein. In einem ersten Schritt aktivieren sie eine spezielle Familie von Transkriptionsfaktoren – wissenschaftlich NFAT genannt für nuclear factor of activated T-cells. Diese wiederum binden im Zellkern an die DNA und leiten damit die Bildung von Zytokinen wie beispielsweise Interleukin-2 ein.
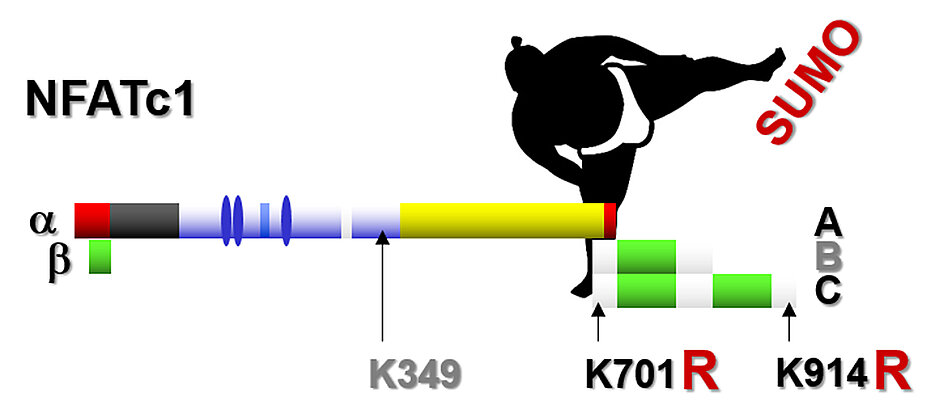
NFAT setzt sich aus vielen Familienmitgliedern zusammen. Diese haben zum Teil überlappende Aufgaben, zum Teil erfüllen sie aber auch ganz unterschiedliche Funktionen. Damit nicht genug: Wie viele andere Proteine in der Zelle auch können sie nach ihrer Synthese noch modifiziert werden, was ihre Funktion individuell anpasst. In der jetzt veröffentlichten Studie haben sich die Wissenschaftlerinnen und Wissenschaftler speziell für eine Modifikation des „Familienmitglieds“ NFATc1 interessiert, die als Sumoylierung bezeichnet wird.
Punktmutationen, die einen Vorteil bringen
„Die Sumoylierung spielt in verschiedenen zellulären Prozessen eine Rolle, beispielsweise beim Kerntransport, beim geplanten Zelltod oder als antiviraler Mechanismus“, erklärt Friederike Berberich-Siebelt. Bei verschiedenen Krankheiten wie etwa Krebs und Infektionen mit Herpesviren ist zudem eine fehlerhafte Sumoylierung beobachtet worden.
In der jetzt veröffentlichten Studie haben die Wissenschaftler mit Versuchstieren gearbeitet, die zwei eigentlich unbedeutende Punktmutationen im NFATc1-Gen aufwiesen, welche jedoch die Sumoylierung verhindern. Ein Schaden ist das nicht unbedingt: „Die Nachkommen dieser Tiere sind vollkommen gesund. Es ist sogar so, dass das veränderte NFATc1 spezielle Signale vermittelt, die zumindest im Tiermodell die klinischen Symptome der Multiplen Sklerose reduzieren“, erklärt Berberich-Siebelt. Und wenn T-Zellen, die diese Veränderungen tragen, bei einer Stammzelltransplantation zum Einsatz kommen, sind diese T-Zellen wesentlich weniger aggressiv gegen die Gewebe der Empfängertiere als „normale“ Zellen.
Grundlagenforschung, die fasziniert
Molekularbiologisch sei dieser Effekt auf ein Mehr an Interleukin-2 zu Beginn der Immunreaktion zurückzuführen. „Interleukin-2 wirkt der Differenzierung zu entzündlichen T-Zellsubtypen entgegen und unterstützt gleichzeitig sogenannte regulatorische T-Zellen“, so die Autoren der Studie. Gut möglich, dass diese Entdeckung Auswirkungen auf zukünftige Stammzelltransplantation hat, bei denen auch T-Zellen übertragen werden. Wenn dabei T-Zellen zum Einsatz kommen, bei denen NFATc1 nicht sumoyliert wird, könnte dies heftige Nebenwirkungen eventuell verhindern – dann wäre die Punktmutation „eine kleine Modifikation mit großer Wirkung“, wie Berberich-Siebelt sagt.
Um das genauer zu untersuchen, werden Berberich-Siebelt und ihr Team weiter an den Möglichkeiten einer therapeutischen Umsetzung forschen im Rahmen des von der Deutschen Forschungsgemeinschaft (DFG) finanzierten Sonderforschungsbereichs/Transregio „Steuerung der Transplantat-gegen-Wirt- und Transplantat-gegen-Leukämie-Immunreaktionen nach allogener Stammzelltransplantation“. „Wir wollen ausloten, ob man die Genschere CRISPR/Cas9 an humanen T-Zellen ansetzen kann, damit sie während einer hämatopoietischen Stammzelltransplantation gerade das richtige Maß an Aktivität zeigen“, so die Wissenschaftlerin.
Aber auch unabhängig von diesen möglichen Konsequenzen für einen therapeutischen Einsatz sind die neuen Erkenntnisse bedeutsam. „Für uns ist es grundsätzlich interessant, die Feinregulation in Zellen zu verstehen, wie in diesem Fall die T-Zellrezeptor-Signalgebung und die Funktion der NFAT-Familienmitglieder und ihrer Isoformen“, sagt Berberich-Siebelt. Sie findet die jetzt veröffentlichten Ergebnisse „faszinierend“. Schließlich mussten die Wissenschaftler in diesem Fall nicht, wie so oft sonst in der Forschung, ein Gen ausschalten oder im Übermaß aktivieren. Stattdessen reichten zwei eigentlich harmlose Punktmutationen und nur subtile direkte Auswirkungen aus, um am Ende den Schalter von Entzündung, Autoimmunität und Abstoßung auf Toleranz umlegen zu können. Eine kleine Schwerpunktverschiebung zu Beginn der Immunreaktion habe dafür genügt.
Förderer
Die beschriebenen Arbeiten wurden durch ein Schwerpunktprogramm der DFG, die Wilhelm Sander-Stiftung und das Interdisziplinäre Zentrum für Klinische Forschung (IZKF) der Medizinischen Fakultät der Universität Würzburg finanziell unterstützt.
Originalpublikation
Lack of NFATc1 SUMOylation prevents autoimmunity and alloreactivity. Yin Xiao, Musga Qureischi, Lena Dietz, Martin Vaeth, Subrahmanya D. Vallabhapurapu, Stefan Klein-Hessling, Matthias Klein, Chunguang Liang, Anika König, Edgar Serfling, Anja Mottok, Tobias Bopp, Andreas Rosenwald, Mathias Buttmann, Ingolf Berberich, Andreas Beilhack, Friederike Berberich-Siebelt. Journal of Experimental Medicine. DOI: 10.1084/jem.20181853
Kontakt
PD Dr. Friederike Berberich-Siebelt, T: +49 931 31 81208, friederike.siebelt@uni-wuerzburg.de