Ein gefährliches Molekül im Alter
08.10.2019Im alternden Gefäßsystem kommt es häufiger zu lebensgefährlichen Situationen wie einem Herzinfarkt. Ein bestimmtes Molekül scheint den Alterungsprozess der Blutgefäße zu begünstigen, wie Würzburger Forscher herausgefunden haben.
Gefäßerkrankungen sind die Todesursache Nummer Eins weltweit – vor allem im höheren Alter. Denn wie alles andere in unserem Körper, altert auch das Gefäßsystem. Diese Alterungsprozesse begünstigen mit anderen Risikofaktoren, wie zum Beispiel hohe Blutfettwerte oder mangelnde Bewegung, die Entwicklung von Gefäßerkrankungen. Damit sind vor allem Gefäßverkalkungen gemeint, die letztlich zu tödlichen Herzinfarkten oder Schlaganfällen führen können. Ein internationales Forschungsteam unter Federführung des Instituts für Anatomie und Zellbiologie der Julius-Maximilians-Universität Würzburg (JMU) hat nun herausgefunden, dass das Protein CEACAM1 die Alterung des Gefäßsystems maßgeblich beeinflusst.
Die Mechanismen, die den Alterungsprozessen im Gefäßsystem zugrunde liegen, sind bislang noch unzureichend erforscht. Umso wichtiger ist nun die Entdeckung des Würzburger Teams für künftige Präventions- und Forschungsmöglichkeiten in der Medizin. Das bestätigt auch die Anatomische Gesellschaft und verlieh daher dem Forschungsteam für diese Entdeckung den „Young Investigator Award“. Publiziert wurden die neuen Ergebnisse erst kürzlich in der Fachzeitschrift „Aging Cell“.
Seit einigen Jahren ist bekannt, dass das Molekül mit dem komplizierten Namen CEACAM1 auf die Struktur der Blutgefäße Einfluss nimmt. „Wir wollten mit unserer Arbeit den genauen Einfluss von CEACAM1 auf die Gefäßalterung feststellen“, erklärt Florian Kleefeldt, wissenschaftlicher Mitarbeiter am Institut für Anatomie und Zellbiologie der JMU.
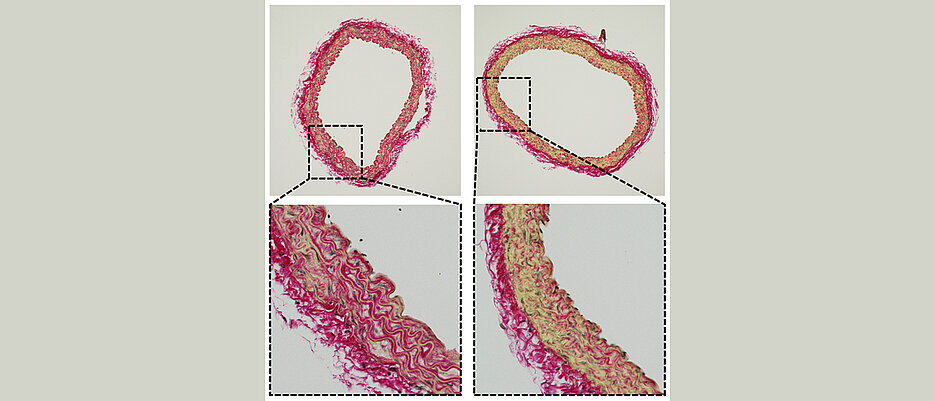
An unterschiedlichen Gefäßproben, bei denen das Molekül entweder vorhanden oder genetisch entfernt worden war, verglichen die Wissenschaftlerinnen und Wissenschaftler schließlich den Zustand der Gefäßwände und konnten so die Auswirkung von CEACAM1 analysieren. Dies wurde auch mithilfe von Tierversuchen bewerkstelligt.
Im Alter mehr CEACAM1 in der Gefäßwand
Es hat sich gezeigt, dass CEACAM1 gleich mehrfach die Gefäßalterung begünstigt. Durch eine gesteigerte Durchlässigkeit der innersten Gefäßwandschicht trägt es zu einer Entzündung des Gefäßes bei. Zudem führt es durch Fibrosierung zu narbenähnlichen Strukturen in den Gefäßwänden, sogenannten Kollagenablagerungen, die Gefäßverkalkungen fördern. Je älter man ist, desto mehr CEACAM1-Moleküle befinden sich in der Gefäßwand. Der Effekt verstärkt sich somit mit zunehmenden Alter.
Die untersuchten Gefäßproben ohne CEACAM1 erbrachten nun ein eindeutiges Ergebnis: Es zeigen sich deutlich geringere altersabhängige Veränderungen in den Gefäßen. Es gibt also weniger Kollagenablagerungen und die Gefäßwände sind deutlich weniger durchlässig. „Das Gefäßsystem eines 80-Jährigen könnte ohne CEACAM1 so gut sein wie das eines 30-Jährigen“, sagt Kleefeldt überspitzt.
„Wir sind mit unserer Forschung nicht direkt am Herzinfarkt oder Schlaganfall. Hier kommt die Therapie für den Patienten häufig zu spät. Wir sind eine Stufe davor, uns geht es bei dieser Forschungsfrage um die Prävention“, erklärt Kleefeldt. „Wir hoffen, dass diese Erkenntnisse in Zukunft neue Behandlungsoptionen ermöglichen, die bereits wirken, bevor es zur Gefäßerkrankung und dem darauffolgenden oft tödlichen Herzinfarkt oder Schlaganfall kommt.“
Kontakt
Florian Kleefeldt, Lehrstuhl II, Institut für Anatomie und Zellbiologie, Universität Würzburg, T +49 (931) 31 80681, florian.kleefeldt@uni-wuerzburg.de