Mini-Organe enthüllen Strategien aggressiver Bakterien
06/17/2025Ein internationales Forschungsteam hat entschlüsselt, wie die aggressiven Shigella-Bakterien den Darm besiedeln. Dabei kamen im Labor entwickelte Mini-Organe zum Einsatz.
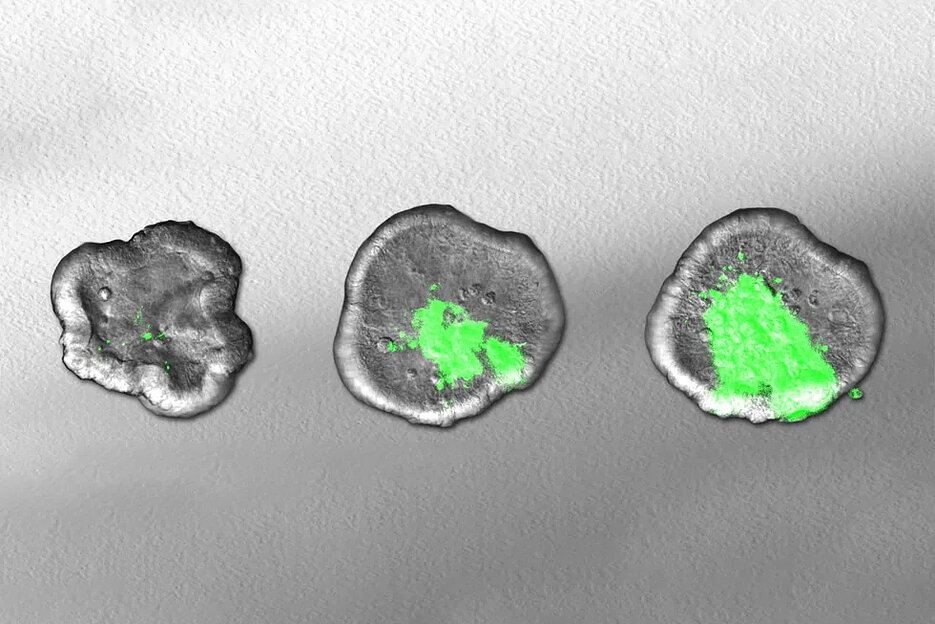
Wie machen Bakterien den Menschen krank? Das herauszufinden, ist keine einfache Angelegenheit. Im Labor gezüchtete Mini-Organe, sogenannte Organoide, können dabei helfen: Mit ihnen lässt sich gut nachvollziehen, wie Mikroben die Darmschleimhaut besiedeln. Das zeigen Forschende in einer neuen Studie, die in Nature Genetics veröffentlicht wurde.
Die Studie stammt von einem Team des Helmholtz-Instituts für RNA-basierte Infektionsforschung (HIRI) in Würzburg – einem Standort des Braunschweiger Helmholtz-Zentrums für Infektionsforschung in Kooperation mit der Universität Würzburg (JMU) – und der Universität Uppsala.
Das Team konzentrierte sich auf Shigella flexneri. Dieses Bakterium verursacht beim Menschen schwere Darmentzündungen und ist jährlich für zahlreiche Todesfälle verantwortlich, besonders bei Kleinkindern.
Alle Gene kartiert, die für die Infektion nötig sind
„Unsere Ergebnisse liefern ein realistischeres Bild der Faktoren, die die Besiedlung des Darms mit Shigella beeinflussen. Künftig könnten sie neue medizinische Behandlungsansätze ermöglichen“, sagt Lars Barquist, assoziierter Wissenschaftler am HIRI, Professor an der Universität Toronto in Kanada und Ko-Seniorautor der Studie.
„Zum ersten Mal konnten wir die Gene kartieren, die Shigella für eine Infektion braucht – und zwar mithilfe eines menschlichen Modells, das echtes Darmgewebe imitiert. Die Studie zeigt außerdem, dass sich gezüchtete menschliche Mini-Organe zur Untersuchung verschiedener schwerer Infektionen eignen – insbesondere solcher, bei denen bislang fehlende Tiermodelle die Forschung erschwert haben“, so Maria Letizia Di Martino von der Universität Uppsala, die die Entwicklung des experimentellen Systems leitete.
Darmmodelle aus Stammzellen entwickelt
Shigella-Bakterien sind invasive Krankheitserreger. Sie greifen das Körpergewebe mit verschiedenen „Waffen“ an, um in die Darmschleimhaut einzudringen und die Funktionen des körpereigenen Immunsystems zu beeinflussen.
In der Studie konzentrierten sich die Forschenden darauf, die Gene zu identifizieren, die für die Produktion dieser Waffen verantwortlich sind. Die dafür verwendeten Darm-Organoide entwickelten sie aus Stammzellen, die aus übrig gebliebenem Gewebe von chirurgischen Eingriffen stammten. Mit einer Methode, bei der einzelne Gene gezielt ausgeschaltet werden, testeten sie, welche Auswirkungen die Veränderungen auf die Fähigkeit von Shigella haben, das menschliche Darmmodell zu infizieren.
Goldgrube für die Entwicklung neuer Therapien
Besonders überraschend war die Entdeckung, dass bestimmte Veränderungen an Transferribonukleinsäuren (tRNAs) die Aktivität des Typ-III-Sekretionssystems steuern können – das ist ein komplexer Apparat, mit dem Bakterien ihre krankmachenden Eigenschaften entfalten. Damit sei nun ein dritter grundlegender Mechanismus zur Steuerung dieses Apparats bekannt, erklärt Laura Jenniches. Sie ist Postdoktorandin im Barquist-Labor und führte die statistische und computergestützte Analyse durch.
„Shigella verfügt über etwa 5.000 Gene, aber wir haben herausgefunden, dass nur etwa 100 davon notwendig sind, um Gewebe zu besiedeln und aggressive Infektionen zu verursachen. Diese Liste ist eine Goldgrube für das Verständnis des Infektionsverlaufs und die Entwicklung neuer Therapien, die das krankmachende Verhalten der Bakterien gezielt ausschalten können“, sagt Mikael Sellin. Er ist Professor an der Universität Uppsala und ein weiterer leitender Autor der Studie. Die in der Studie eingesetzte Screening-Technologie sei auf viele weitere Erreger übertragbar und ermögliche künftig realitätsnahe Studien an menschlichen Geweben.
Lars Barquist blickt voraus: „Diese Studie schafft die technischen Voraussetzungen für die Untersuchung zahlreicher Krankheitserreger in realistischen Organoid-Modellen, die zentrale Aspekte der menschlichen Physiologie im Labor nachbilden.“
Förderung
Unterstützt wurde die Studie aus Mitteln der Europäischen Gesellschaft für Klinische Mikrobiologie und Infektionskrankheiten (ESCMID), der Carl-Trygger-Stiftung, der Clas-Groschinsky-Gedächtnisstiftung, des Bayerischen Staatsministeriums für Wissenschaft und Kunst (über bayresq.net), des Schwedischen Wissenschaftsrats, der Schwedischen Stiftung für Strategische Forschung sowie durch Kempestiftelserna und das SciLifeLab Fellows-Programm.
Publikation
A scalable gut epithelial organoid model reveals the genome-wide colonization landscape of a human-adapted pathogen. Nature Genetics, 12. Juni 2025, DOI: 10.1038/s41588-025-02218-x