Schnellere Bestimmung von Protein-Affinitäten
29.01.2021Proteininteraktionen können jetzt noch effektiver analysiert werden: Ein Phänomen namens Temperature Related Intensity Change (TRIC) macht es möglich, hohe Intensitäten von Bindungssignalen auch mit geringsten Probenmengen zu erreichen. Unsere AG Maric etablierte eine Methode, mit der sich Proteinkomplexe in komplexen Netzwerken wie der DNA-Transkription untersuchen lassen.
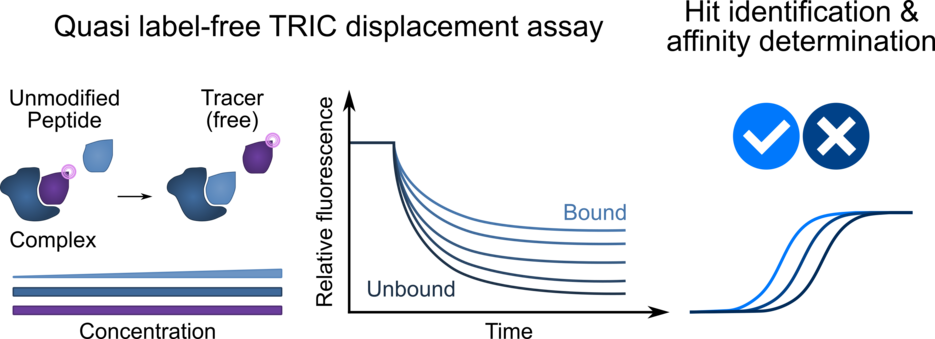
Beschränkungen der derzeit verfügbaren Methoden
Protein-Protein-Interaktionen (PPIs) spielen bei nahezu allen physiologischen Prozessen eine entscheidende Rolle. Um neue therapeutische Ansätze zu erforschen, ist es wichtig, diese Interaktionen zu quantifizieren und zu verstehen. Bisher wurden verschiedene Ansätze zur Quantifizierung von Protein-Interaktionen entwickelt, deren Anwendung jedoch typischerweise durch geringen Durchsatz und aufwändige Probenvorbereitung erschwert wird.
Kombination aus schneller Synthese und schneller Bindungsauswertung
Wissenschaftlerinnen und Wissenschaftler aus der Forschungsgruppe von Dr. Hans Michael Maric zeigten nun gemeinsam mit Experten von Nanotemper Technologies in München, wie die genannten Einschränkungen überwunden werden können.
"Wir haben einen Aufbau etabliert, der Hochdurchsatzsynthese und Bindungsevaluierung kombiniert", sagt Maric. Das neue Setup ermöglicht die präzise Bestimmung der Bindungsaffinitäten von unmodifizierten Liganden in Lösung. "Indem es Einblicke auf molekularer Ebene in Lösung liefert, ergänzt das neue Setup unseren Array-basierten Ansatz in einer Genauigkeit, den wir bisher nur mit aufwändigen Low-Throughput-Techniken erreichen konnten", erklärt Maric.
Größenunabhängige Messungen mit TRIC
Im Gegensatz zu anderen, weit verbreiteten Hochdurchsatz-Quantifizierungsansätzen ist die vorgestellte TRIC-Messung weitgehend unabhängig von der Ligandengröße. "Durch die Verdrängung eines fluoreszenten Tracers ermöglicht dieser Ansatz nicht nur die Messung von unmodifizierten Liganden, sondern verstärkt auch das Signal im Vergleich zu anderen Messmethoden", erklärt Clemens Schulte.
Automatisierung und Kommerzialisierung
Amit Jean Gupta von Nanotemper Technologies ist für die Kommerzialisierung des "Dianthus" verantwortlich, der weitgehend automatisierte TRIC-Messungen ermöglicht. "Konventionelle Microscale Thermophoresis (MST)-Messungen erfordern die Verfolgung der molekularen Bewegung entlang eines Temperaturgradienten in einem Gefäß, das turbulente Strömungen verhindert. Durch die ausschließliche Verwendung des TRIC-Prinzips konnten wir die Volumina reduzieren und eine vollständige Kompatibilität mit Mikrotiterplatten erreichen, was eine Automatisierung und einen höheren Durchsatz ermöglicht, während die Vorteile der konventionellen MST-Messungen erhalten bleiben. Die Arbeit des Maric-Teams etabliert TRIC-Messungen als einen praktikablen Ansatz zur PPI-Quantifizierung mit hohem Durchsatz und stellt eine wichtige Referenz für zukünftige Anwendungen dar", sagt Amit Gupta.
Weitere Forschung erforderlich
Im Rahmen des aktuellen Setups werden zunächst Tausende von Peptiden durch ein automatisiertes System synthetisiert und dann direkt für die Hochdurchsatz-Bindungsauswertung eingesetzt. Hier könnten zusätzliche, universelle Peptid-Reinigungsschritte die Robustheit, Sensitivität und den Vorhersagewert der Methode erheblich verbessern, insbesondere für Peptide, die 20 Aminosäuren überschreiten. "Die erhöhte Miniaturisierung und Automatisierung hat unsere Fähigkeit zur Entschlüsselung komplexer Protein-Protein-Interaktionsnetzwerke weiter verbessert. Bei iterativer Anwendung ermöglicht unsere Technologie die Entwicklung von hochspezifischen Bindern. Wir werden unseren Aufbau nutzen, um spezifische Proteinkomplexe in komplexen Netzwerken wie der DNA-Transkription und der Funktion der neuronalen Synapse zu untersuchen und anzusteuern", schließt Maric.
Publikation
Clemens Schulte, Vladimir Khayenko, Noah Frieder Nordblom, Franziska Tippel, Violetta Peck, Amit Jean Gupta, Hans Michael Maric,High-throughput Determination of Protein Affinities using Unmodified Peptide Libraries in Nanomolar Scale. iScience, January 2021, DOI: 10.1016/j.isci.2020.101898
Kontakt
Dr. Hans Michael Maric (Rudolf-Virchow-Zentrum, Universität Würzburg)
Tel.: +49 931 31-85371, Hans.Maric@uni-wuerzburg.de
Clemens Schulte (Rudolf-Virchow-Zentrum, Universität Würzburg)
Tel.: +49 931 31-89734, Clemens.Schulte@uni-wuerzburg.de