Neue Erkenntnisse über die molekulare Wirkungsweise des Anti-Malaria-Wirkstoffs Artemisinin
28.01.2019Forscher des Rudolf-Virchow-Zentrums der Universität Würzburg haben die Wirkungsweise von Artemisininen auf molekularer Ebene aufgeklärt. Die neuen Erkenntnisse haben unter anderem das Potenzial, die Entwicklung von Medikamenten gegen Krankheiten wie Alzheimer, Schizophrenie und Epilepsie voranzubringen. Die Studie wurde in der Fachzeitschrift Neuron veröffentlicht.
Artemisinin wird aus den Blättern und Blüten des Einjährigen Beifußes (Artemisia annua) gewonnen und bereits seit Jahrhunderten in der traditionellen chinesischen Medizin eingesetzt. Die Wirksamkeit wurde von der chinesischen Forscherin Tu Youyou erforscht und durch die Vergabe des Nobelpreises honoriert. Artemisinin und seine halbsynthetischen Derivate – man spricht zusammenfassend von Artemisininen – werden zur Behandlung der tropischen Infektionskrankheit Malaria eingesetzt. Außerdem beeinflussen diese Moleküle auch verschiedene zelluläre Prozesse beim Menschen. So sind Artemisinine zum Beispiel in der Lage, das Immunsystem gegen mehrere Krebsarten zu aktivieren oder die Differenzierung der alpha-Zellen in der Bauchspeicheldrüse zu regulieren, was potenziell in der Diabetes-Therapie von Nutzen sein könnte.
Molekulare Mechanismen bislang unbekannt
„Obwohl diese klinisch zugelassene Wirkstoffgruppe durchaus verbreitet und teilweise schon seit Jahrhunderten eingesetzt wird, war bislang unklar, welche molekularen Mechanismen den entsprechenden zellulären Aktivitäten, also zum Beispiel der Zielproteinerkennung und -modulation, zugrunde liegen“, erläutert Dr. Vikram Kasaragod. Der Postdoktorand in der Forschungsgruppe von Prof. Hermann Schindelin am Rudolf-Virchow-Zentrum ist der Erstautor des Artikels in der renommierten Zeitschrift „Neuron“ und sorgt mit dieser Forschungsarbeit für einen wesentlichen Erkenntnisgewinn (siehe auch die begleitende Perspektive / Preview von Ryan Hibbs in derselben Ausgabe von „Neuron“).
Modell der Regulation der Neurotransmission entwickelt
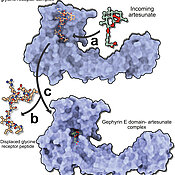
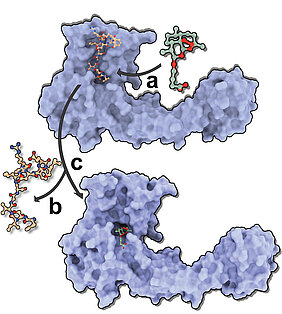
Der Strukturbiologe löste als erster die Kristallstrukturen von zwei verschiedenen Artemisinin-Derivate – Artesunat und Artemether – in einem Komplex mit Gephyrin. Durch die Bindung an inhibitorische Glyzin- und GABAA-Rezeptoren fungiert Gephyrin als zentrales Gerüstprotein inhibitorischer Postsynapsen im Zentralnervensystem von Säugetieren. Gephyrin wurde erst vor kurzem als Artemisinin-Zielprotein identifiziert. Die Ergebnisse zeigen deutlich, wie Artemisinine auf die universelle Rezeptorbindungstasche in Gephyrin abzielen und mit den inhibierenden Neurotransmitterrezeptoren um eine überlappende Bindungsstelle konkurrieren (siehe Abbildung). Diese neuen Erkenntnisse könnten somit auch als wirksames Instrument für die Aufklärung der Physiologie des menschlichen Gehirns dienen.
Laut Kasaragod bilden die Kristallstrukturen zusammen mit biochemischen, elektrophysiologischen und in vivo Daten ein umfassendes Modell der Regulation der inhibitorischen Neurotransmission durch Artemisinine. Mit diesem Modell lassen sich nach seinen Worten die Wechselwirkungen zwischen Proteinen und Medikamenten eindeutig beschreiben.
Wichtiger Schritt für die Entwicklung von Medikamenten
„Unsere Daten liefern nicht nur eine solide Grundlage für das Verständnis, wie Artemisinine von einem Zielmolekül erkannt werden, sondern werden Forschern auch helfen, diese Wirkstoffe zu hochspezifischen Modulatoren von Gephyrin zu entwickeln und zu optimieren. Diese Modulatoren könnten zukünftig bei der Behandlung von neurologischen Krankheiten wie Morbus Alzheimer, Schizophrenie und Epilepsie eine wichtige Rolle spielen“, erläutert Schindelin, der Leiter der Studie.
Die in Neuron veröffentlichten Daten sind das Ergebnis einer interdisziplinären Zusammenarbeit mit anderen Forschern der Universität Würzburg, des Universitätsklinikums Hamburg und der Universität Kopenhagen.
Offene Stellenanzeige: PhD Student Positions in Protein Structure and Function (Bewerbungsfrist: 30.04.2019)
Publikation
Vikram Babu Kasaragod, Torben Johann Hausrat, Natascha Schaefer, Maximilian Kuhn, Nikolaj Riis Christensen, Ingrid Tessmer, Hans Michael Maric, Kenneth Lindegaard Madsen, Christoph Sotriffer, Carmen Villmann, Matthias Kneussel and Hermann Schindelin: Elucidating the Molecular Basis for Inhibitory Neurotransmission Regulation by Artemisinins. Neuron (2019) Published: January 28, 2019 DOI:https://doi.org/10.1016/j.neuron.2019.01.001 Altmetric Publikation
Personen
Dr. Vikram Kasaragod ist Postdoktorand in der Forschungsgruppe von Prof. Dr. Hermann Schindelin am Rudolf-Virchow-Zentrum für Experimentelle Biomedizin der Universität Würzburg.
Prof. Dr. Hermann Schindelin ist Professor für Strukturbiologie und Biochemie und leitet seit 2006 eine Forschungsgruppe am Rudolf-Virchow-Zentrum für Experimentelle Biomedizin der Universität Würzburg.
Kontakt
Dr. Vikram Kasaragod (AG Schindelin, Rudolf-Virchow-Zentrum) vikram.kasaragod@virchow.uni-wuerzburg.de
Prof. Dr. Hermann Schindelin (Rudolf-Virchow-Zentrum)
Tel. 0931 31 80382, hermann.schindelin@virchow.uni-wuerzburg.de
Dr. Daniela Diefenbacher (Pressestelle, Rudolf-Virchow-Zentrum)
Tel. 0931 3188631, daniela.diefenbacher@uni-wuerzburg.de